AEM Wasserelektrolyse: Wie funktioniert das eigentlich?
Als der führende Hersteller von AEM-Elektrolyseuren fühlen wir uns verpflichtet alles über die Funktionsweise der AEM-Elektrolyse zu teilen. Was also bedeutet AEM und wie genau funktioniert diese Technologie?
Grüner Wasserstoff gehört mittlerweile zu den vielversprechendsten Energieträgern, um fossile Brennstoffe in vielen Bereichen vollständig zu ersetzen. Produziert wird er mittels erneuerbarer Energien und Wasser.
Im Laufe der letzten Jahrhunderte wurden bereits verschiedene Technologien zur Herstellung grünen Wasserstoffs entwickelt. Innerhalb dieser Entwicklungen fehlte aber ein wichtiges Puzzleteil, um grünen Wasserstoff in den benötigten Mengen bezahlbar zu produzieren.
Mit der von uns entwickelten Anionenaustauschmembran-Technologie (AEM) zur Wasserelektrolyse ist es nun jedoch möglich, dieses Puzzle zu vervollständigen.
Bevor wir uns aber die AEM genauer ansehen, müssen wir zunächst eine Frage beantworten:
Warum können wir Energie in Wasserstoff speichern?
Die Wasserelektrolyse ist eine Reaktion, bei der Wassermoleküle in Wasserstoff und Sauerstoff gespalten werden.
Dabei handelt es sich um einen endothermen Prozess. Das bedeutet, dass Energie in Form von chemischen Bindungen im Wasserstoff aufgenommen und gespeichert werden kann.
Die umgekehrte Reaktion – wenn also Wasserstoff und Sauerstoff Wassermoleküle bilden – ist dagegen eine exotherme Reaktion, bei der Energie an die Umgebung abgegeben wird.
Durch den Kreislauf der endothermen Wasserelektrolyse und der anschließenden exothermen Wasserbildungsreaktion können wir erneuerbare Energie in grünem Wasserstoff speichern – es bedarf keiner fossilen Brennstoffe und es entstehen dabei keine Kohlendioxidemissionen.
Was ist nun das Besondere an der AEM?
Um die Mechanismen der AEM-Elektrolyse genauer zu verstehen, hilft es, zuerst einen Blick auf die wichtigste Komponente in einem AEM-Elektrolyseur zu werfen: den AEM-Stack – in diesem findet die Wasserspaltungsreaktion statt.
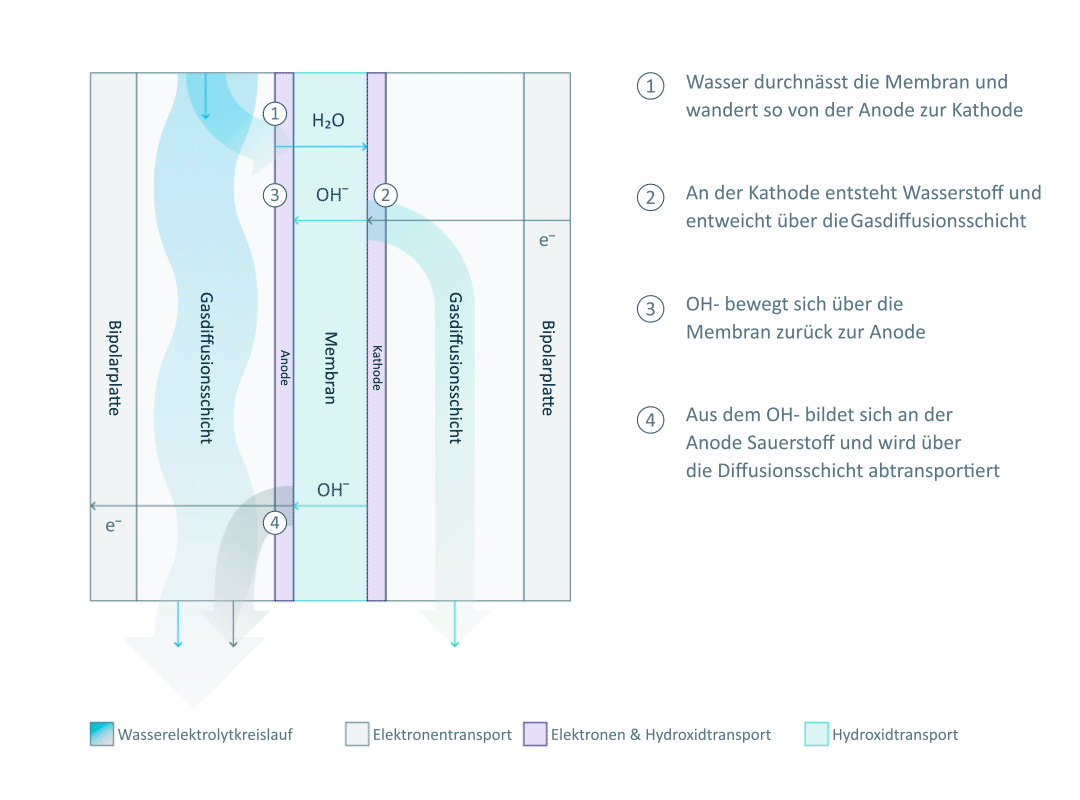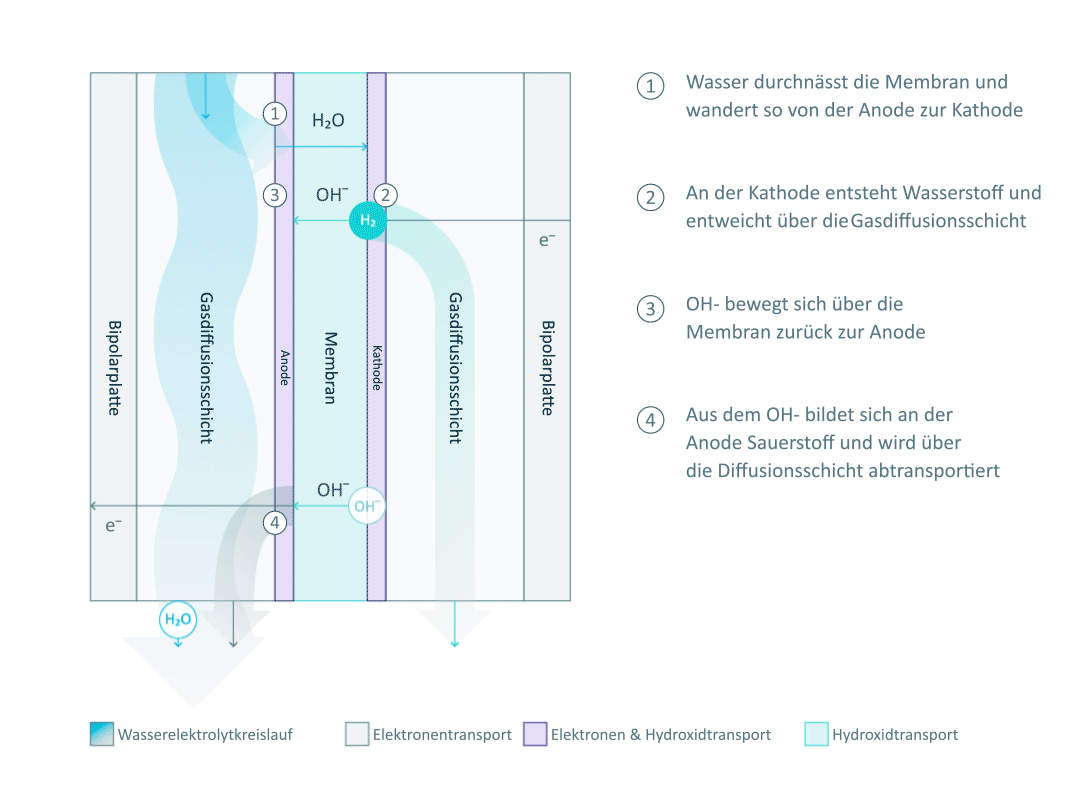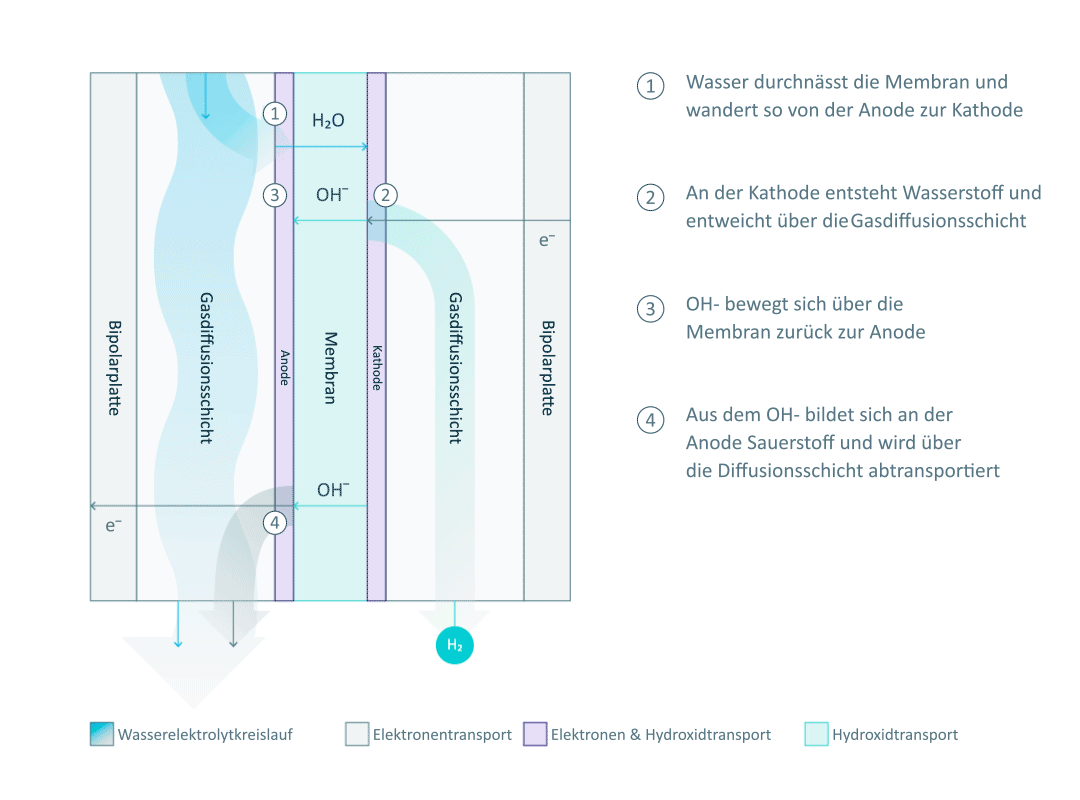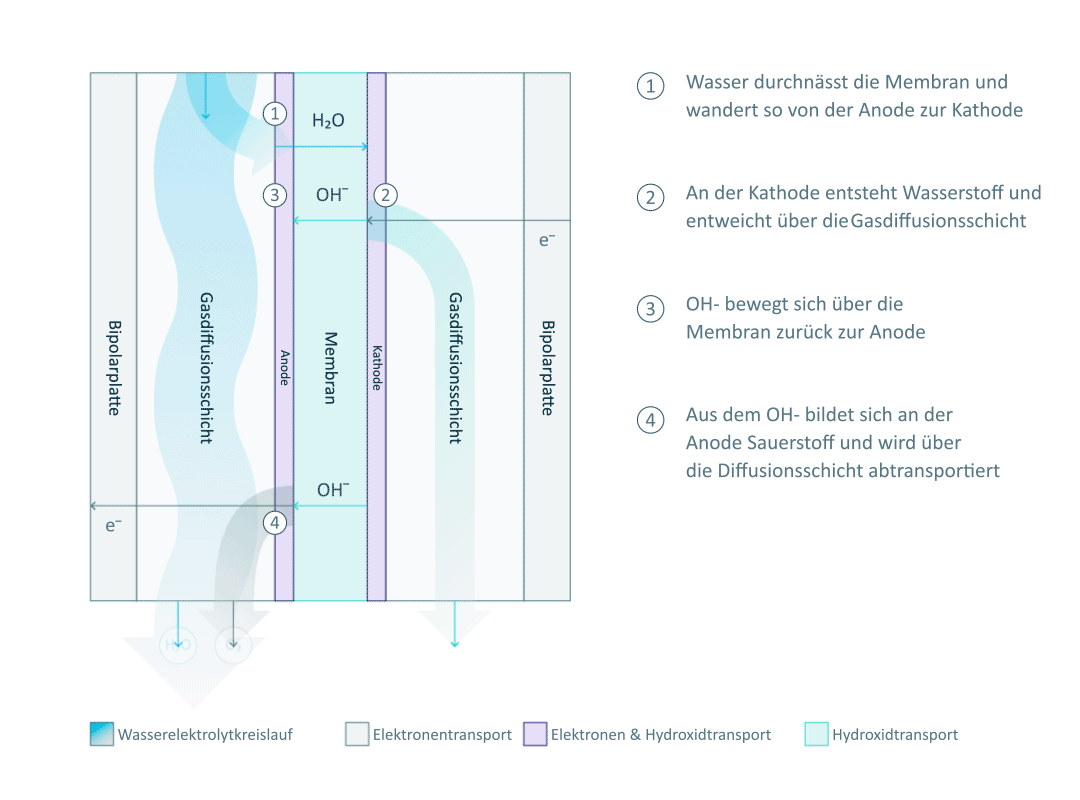
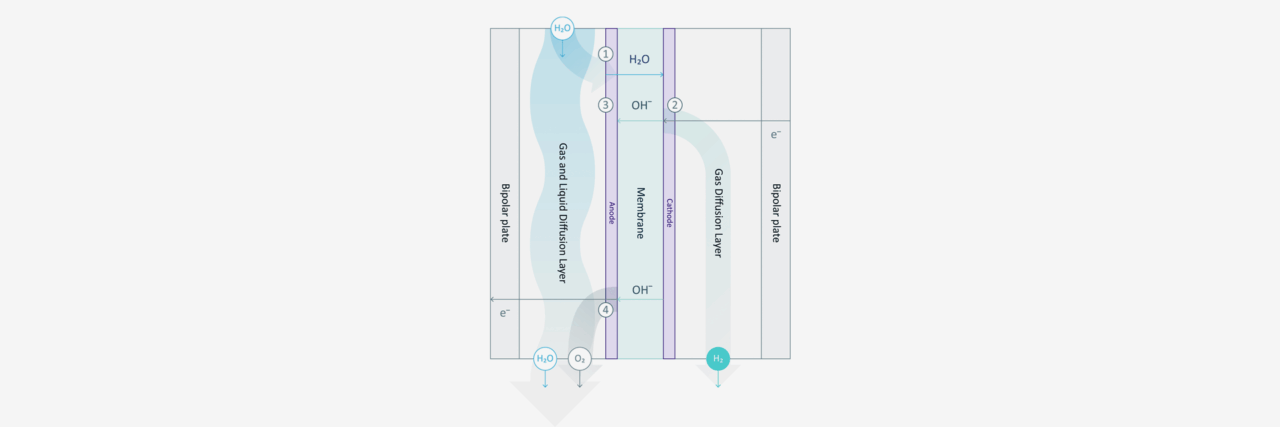
Wie du in der Abbildung siehst, ist die Einzelzelle durch die Anionenaustauschmembran in zwei Halbzellen unterteilt. Jede Halbzelle besteht aus einer Elektrode, einer Gasdiffusionsschicht und einer Bipolarplatte.
Mehrere Einzelzellen werden durch die Bipolarplatte miteinander verbunden und bilden so den AEM-Stack.
Diese Anordnung der Halbzellen in einem AEM-Elektrolyseur ermöglicht die Erzeugung von Wasserstoff und Sauerstoff bei einem Druck von 35 bar. 1 bar. Durch den Druckunterschied zwischen den Halbzellen wird verhindert, dass der erzeugte Sauerstoff in die Hochdruck-Halbzelle übergeht, wodurch eine sehr hohe Reinheit des Wasserstoffs (99,9 %) gewährleistet ist.
Wir werden aus H₂O dann H?
Der Wasserelektrolyt, der nur 1 % Kaliumhydroxid (KOH) enthält, zirkuliert ausschließlich in der Anodenhalbzelle und benetzt die Membran, während die Kathodenseite trocken bleibt. Der in der Kathodenhalbzelle erzeugte Wasserstoff hat somit nur einen sehr geringen Feuchtigkeitsgehalt. Daher ist es wichtig zu beachten, dass in der Kathodenhalbzelle kein KOH zu finden ist.
Die Wassermoleküle wandern durch die Membran, werden an der Kathode reduziert und erzeugen so Wasserstoff. Die Stromversorgung aus dem externen Stromkreis wird genutzt, um eine elektrische Potenzialdifferenz an der Grenzfläche zwischen Elektrolyt und Elektrode zu erzeugen.
Die Potenzialdifferenz treibt dann die Wasserstoffentwicklungsreaktion (HER) durch Elektronenübertragung (e-) an:
4H2O + 4e- → 4OH- + 2H2
Der erzeugte Wasserstoff wird anschließend über die Gasdiffusionsschicht an die Ausgangsleitung abgegeben. Geeignete HER-Katalysatoren an der Kathode erleichtern den Prozess, indem sie die Energiebarriere der Reaktion herabsetzen.
In der mildalkalischen Umgebung des AEM-Elektrolyseurs kehrt das verbleibende Hydroxidion (OH-) aus der HER über die Membran in die Anodenhalbzelle zurück. Das ausgetauschte OH- ist ein Anion - und dieses gibt der AEM ihren Namen.
Und was ist dabei der Unterschied zwischen AEM- und PEM-Elektrolyse?
Zum Vergleich: In einem Protonenaustauschmembran-Elektrolyseur (PEM) wird das Proton (H+) in einer stark sauren Umgebung durch die PEM transportiert. Hierfür benötigt der PEM-Elektrolyseur Platingruppenmetalle (PGM) als Katalysatoren und kostspielige Titan-Bipolarplatten, um die stark korrosive und saure Umgebung zu überstehen. Im AEM-Elektrolyseur reichen hingegen Nicht-PGM-Katalysatoren und Stahl-Bipolarplatten für eine effektive Wasserstoffproduktion vollkommen aus.
Die verdünnte KOH-Lösung in einem AEM-Elektrolyseur ist zudem sicherer zu handhaben als der Elektrolyt mit einem pH-Wert von 14 in einem TA-Elektrolyseur.
Wie viel Wasserstoff bekommt man nun aus einem AEM-Elektrolyseur?
Nachdem das OH- zur Anodenseite eines AEM-Elektrolyseurs zurücktransportiert wurde, wird es durch die Sauerstoffentwicklungsreaktion (OER) verbraucht:
4OH- → 2H2O + O2 + 4e-
Für je zwei Einheiten Wasserstoff wird eine Einheit Sauerstoff durch Übertragung von vier Einheiten Elektronen erzeugt. Daher kann die Konzentration des OH- im Elektrolyten durch ständige Zufuhr von Wasser konstant bleiben, ohne dass mehr KOH zugesetzt wird.
Die OER wird durch die Potenzialdifferenz an den katalytischen Stellen auf der Anode angetrieben und der erzeugte Sauerstoff wird über die Gasdiffusionsschicht zusammen mit dem Elektrolytkreislauf aus der Anodenhalbzelle entfernt.
Mit der AEM-Wasserelektrolyse können wir unseren modularen Elektrolyseuren so 500 NL grünen Wasserstoff pro Stunde mit einer Reinheit von 99,9 % (99,999 % nach Trocknung) bei 35 bar Druck aus 0,4 l Wasser und 2,4 kWh erneuerbarer Energie produzieren.
Noch Fragen?
Wenn du jetzt wissen möchtest, wie du die Erzeugung von grünem Wasserstoff durch AEM-Elektrolyse auch für dich nutzen kannst, bist du herzlich eingeladen, dich mit unserem Team in Verbindung zu setzen – und natürlich auch, wenn du doch noch weitere Fragen zu unseren AEM-Elektrolyseuren hast.
by Jingwen Wang
Erfahre noch mehr über uns - z.B. über unsere Arbeit mit dem Elektronenmikroskop.